Aspectos generales
¿Por qué hacer el análisis?
Para determinar si un antibiótico o antifúngico concreto va a resultar efectivo en frenar el crecimiento de la bacteria u hongo causante de la infección.
¿Cuándo hacer el análisis?
Se recomienda en las siguientes situaciones:
- Cuando el tratamiento no está siendo efectivo
- Como seguimiento frente a un cultivo bacteriano o fúngico positivo.
- Cuando se ha tomado una muestra de la zona infectada y en el cultivo de la misma se ha aislado una o más tipos de bacteria u hongo.
¿Qué muestra se requiere?
Una muestra de cultivo puro de la bacteria u hongo aislado de la muestra de la zona infectada.
¿Es necesario algún tipo de preparación previa?
No requiere ninguna preparación previa.
¿Qué es lo que se analiza?
Nuestro sistema inmune ha evolucionado para combatir aquellos microorganismos (bacterias, hongos, parásitos o virus) que pueden causar enfermedad y coexistir con muchos otros sin generar ningún daño. Cada persona tiene una flora equilibrada, un conjunto de microorganismos que viven en la superficie cutánea y el tracto digestivo. En general, estas pequeñas formas de vida son beneficiosas, ayudan a la digestión de la comida y sirven como barrera contra microorganismos patógenos que pueden provocar enfermedades. En algunas situaciones en las que se produzca un desequilibrio en la flora, que el sistema inmune del paciente esté deprimido o que una herida o factor desencadenante cree una brecha en el sistema inmune puede ocurrir un sobrecrecimiento oportunista de un tipo de flora normal o la entrada de uno o más microrganismos patógenos y provocar una infección.
Cuando el sistema inmune del paciente no es capaz de eliminar el patógeno o de restaurar el equilibrio de la flora habitual por su cuenta es cuando se recomienda el uso de antibióticos. Estos medicamentos (antibióticos, antifúngicos o antivirales) se han desarrollado para combatir los microorganismos responsables de la infección. Van dirigidos contra las diferentes características de los microrganismos, como su capacidad de multiplicarse, su pared celular o su metabolismo. Distintos tipos de antibióticos son efectivos frente a distintos tipos de microorganismos. Algunos son muy específicos, desarrollados para eliminar una familia concreta de bacterias sin afectar al equilibrio de la flora habitual. Otros son los llamados de “amplio espectro”, desarrollados para inhibir el crecimiento de muchos microrganismos diferentes. Cuando estos se emplean, afectan tanto a los microorganismos patógenos como a la flora habitual.
Algunos microorganismos son resistentes a medicamentos antimicrobianos concretos. El estudio de la resistencia a antimicrobianos (o antibióticos si nos referimos a bacterias) se recomienda para determinar si el empleo de un medicamento concreto será efectivo para eliminar o inhibir el crecimiento de un microorganismo que está provocando una infección. En los siguientes apartados se encontrará información acerca de cómo se realiza un estudio de resistencia (también llamado sensibilidad) a antimicrobianos y cómo ocurre esta resistencia, centrado en los medicamentos antibióticos y en las infecciones causadas por bacterias.
¿Qué es un antibiótico?
Un antibiótico es un medicamento que se utiliza para tratar infecciones causadas por bacterias, porque las mata o impide que se multipliquen. Por eso, no es útil frente a virus: no cura el resfriado ni la gripe.
Usarlos incorrectamente cuando no hacen falta no acelera la recuperación y puede provocar efectos adversos y favorecer que aparezcan bacterias resistentes (que dejan de responder al antibiótico). Cuando es necesario, se realiza un antibiograma para ayudar a elegir el antibiótico más adecuado.
¿Qué es la resistencia bacteriana a los antibióticos?
La resistencia es la capacidad de una bacteria de sobrevivir y crecer en presencia de uno o más antibióticos. En esta situación el tratamiento antibiótico no es efectivo y la bacteria resistente continúa causando la infección. En definitiva, es un mecanismo de adaptación de la bacteria para poder crecer y multiplicarse frente a condiciones adversas.
¿Cómo se hacen resistentes las bacterias?
Las bacterias se hacen resistentes a los antibióticos de varias formas:
- Resistencia intrínseca: Algunas bacterias tienen características propias que las hacen resistentes a algunos antibióticos de manera natural.
- Resistencia adquirida: Otras bacterias se vuelven resistentes a un antibiótico cuando son transmitidas un fragmento de material genético de otra bacteria ya resistente. Un modo de hacerlo es mediante los plásmidos. Los plásmidos son fragmentos de ADN bacteriano que pueden transferirse entre bacterias. Algunos plásmidos permiten que la bacteria produzca una enzima que hace que los antibióticos no sean útiles. Cuando el plásmido se inserta en otra bacteria, la resistencia al antibiótico puede extenderse fácil y rápidamente entre las bacterias. Por último, el material genético de una bacteria puede cambiar o mutar espontáneamente y convertirse con ese cambio en una bacteria resistente.
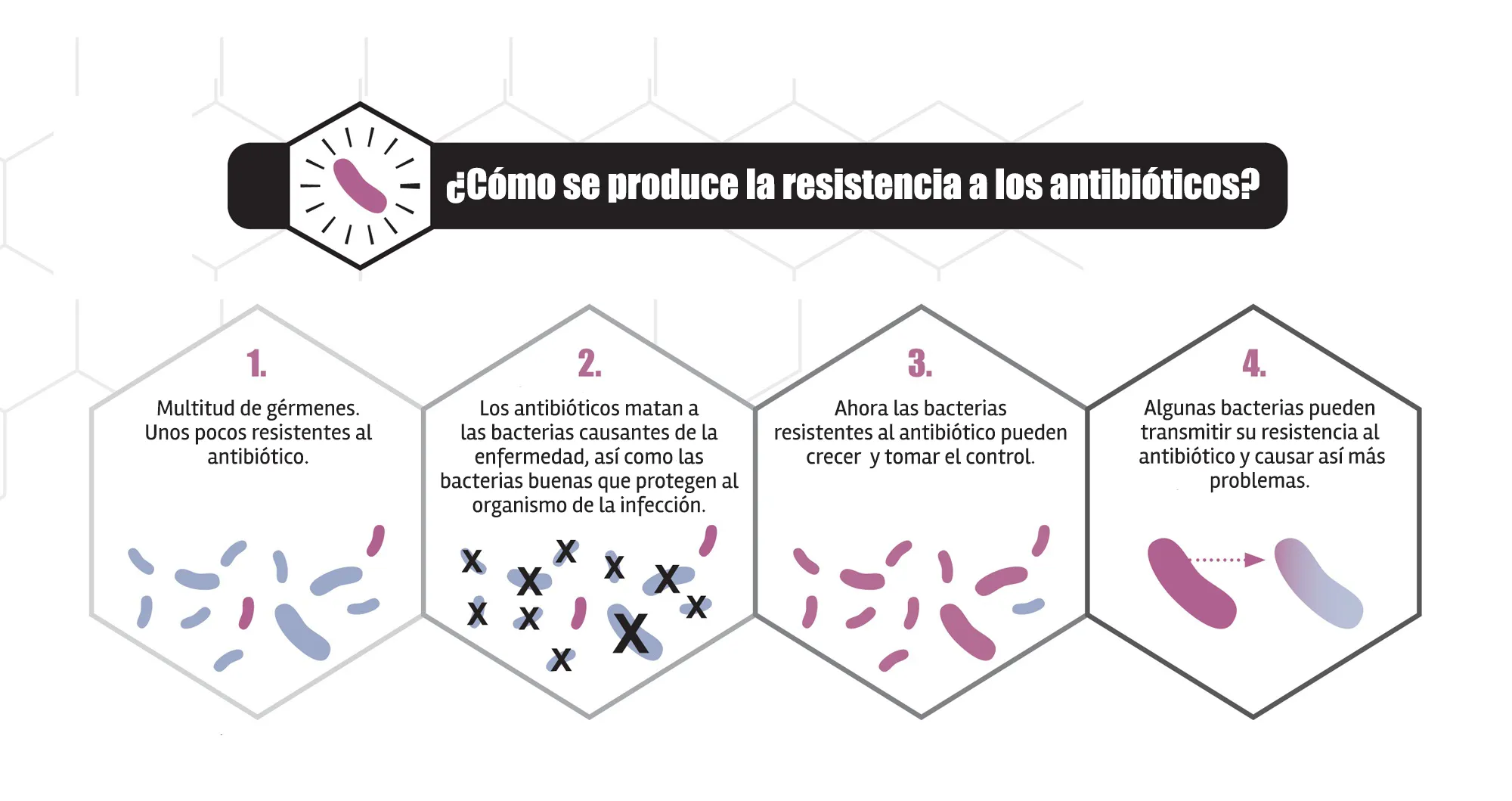
La principal causa de aparición de resistencias en las bacterias es el uso inadecuado de antibióticos. Un antibiótico puede provocar la eliminación de las distintas bacterias que haya en una zona, las beneficiosas y las patógenas. Sin embargo, una reducción de la pauta establecida o el uso del antibiótico incorrecto favorecerá que si alguna de estas bacterias patógenas tiene un mecanismo deresistencia y logra sobrevivir ahora pueda crecer y multiplicarse sin control y empeorar la infección. Ahora, la bacteria patógena resistente se transmitirá a otros individuos y podrá transmitir su mecanismo de resistencia a otras bacterias.
Con el tiempo, las bacterias pueden adquirir más de un tipo de resistencia mediante diferentes mecanismos. Esto puede llevar a las llamadas “superbacterias” o bacterias farmacorresistentes que son resistentes a muchas clases de antibióticos y provocan infecciones difíciles o imposibles de tratar.
Test de resistencia bacteriana a antibióticos
Test de resistencia bacteriana a antibióticos o antibiograma
Cuando se sospecha de una infección bacteriana el médico solicita un “cultivo y test de resistencia (o sensibilidad)”, también conocido como antibiograma, para determinar la causa de la infección. Se llama “sensibilidad” a la capacidad de un determinado antibiótico de eliminar o frenar el crecimiento de una bacteria específica que está provocando una infección. El término “resistencia” se refiere a la incapacidad de ese antibiótico de eliminar una bacteria. Se puede emplear el término “resistente” o ”sensible” a un antibiótico en función de los resultados de este estudio. El estudio de resistencia bacteriana consiste en medir si una bacteria es capaz de crecer o no al enfrentarse a diferentes antibióticos en un entorno controlado como es el laboratorio. Los antibióticos elegidos son aquellos que se utilizan como “primera” o “segunda línea” frente a esa bacteria, es decir, aquellos que se prescriben de manera habitual cuando se detecta esa bacteria como causante de la infección.
El cultivo consiste en incubar la muestra en unas condiciones ricas en nutrientes ya una temperatura que asemeje la corporal durante un periodo de tiempo establecido. Este proceso favorece el crecimiento o replicación de cualquier microorganismo que se encuentre en la muestra recogida. En muestras recogidas de la piel, heces o esputo crecerán microorganismos patógenos y microorganismos normales de la flora habitual. En cambio, en muestras de sangre u orina, donde no existe flora habitual solo se verá crecimiento, si lo hay, de microorganismos patógenos.
La bacteria patógena que ha crecido se aísla, es decir, se separa de cualquier otro microorganismo que esté presente en la muestra y se identifica mediante una variedad de pruebas. Cada bacteria aislada que se sospeche que puede ser la causante de la infección se somete al estudio de resistencia bacteriana para determinar la capacidad de los antibióticos de inhibir su crecimiento. El estudio consiste en incubar la bacteria aislada en presencia de distintos antibióticos de concentración conocida. Se mide la cantidad de crecimiento de la bacteria y se determina cuál de esos antibióticos ha sido efectivo y la concentración a la que se consigue el efecto deseado.
Los resultados para cada antibiótico pueden ser los siguientes:
- Sensible (S): Es probable, aunque no garantizado totalmente, que el antibiótico sea capaz de inhibir al microorganismo patógeno con un régimen de dosificación estándar.
- Sensible, cuando se incrementa la exposición (I): Es probable que el antibiótico sea efectivo si se incrementa la exposición al mismo, es decir, si se emplea una mayor dosis. Es decir, la diferencia entre “S” e “I” es la cantidad de antibiótico empleado para alcanzar una respuesta clínica adecuada.
- Resistente (R): El antibiótico no es efectivo para inhibir el crecimiento del microorganismo.
La clasificación S/I/R se basa en las directrices de EUCAST, el Comité Europeo encargado de emitir y actualizar los criterios clínicos y los puntos de corte de cada antibiótico para cada bacteria.
El tratamiento para esa infección se elige de entre aquellos antibióticos que son “sensibles”. Si ninguno es sensible, se elige el antibiótico clasificado como “Sensible con exposición incrementada”. Este caso puede implicar el empleo de una dosis superior de antibiótico o una mayor duración del tratamiento y, por tanto, un mayor riesgo de efectos adversos.
Si una bacteria se clasifica como “resistente” a todos los antibióticos empleados habitualmente para tratar ese tipo de infección el médico puede prescribir varios antibióticos cuya combinación sea más efectiva frente a la bacteria que el empleo de uno u otro de manera individual. Estos tratamientos pueden ser más costosos, de administración más compleja (intravenosa) y durante un largo periodo de tiempo. Las infecciones provocadas por bacterias resistentes son difíciles de tratar.
¿Existen más pruebas para detectar la resistencia a los antibióticos en el laboratorio?
Para orientar el tratamiento y reducir el uso innecesario de antibióticos, los laboratorios combinan métodos fenotípicos (lo que la bacteria “hace” ante el antibiótico) con pruebas rápidas (para identificar mecanismos concretos de resistencia) y, en situaciones seleccionadas, técnicas moleculares y genómicas (para detectar genes y estudiar brotes).
1) Pruebas fenotípicas (base del antibiograma en la práctica clínica)
Son las más utilizadas para decidir el antibiótico, la dosis y la duración del tratamiento. Se realizan con métodos estandarizados, controles de calidad y puntos de corte que permiten clasificar el aislamiento como S / I / R.
- Difusión en disco (Kirby–Bauer): se siembra la bacteria en una placa y se colocan discos con antibióticos. Tras incubación, se mide el halo donde no crece: cuanto mayor es el halo, más sensible suele ser la bacteria a ese antibiótico.
- Tiras de gradiente (E-test): es una extensión cuantitativa de la difusión. Consiste en una tira con concentraciones crecientes permite leer una CMI aproximada (la concentración mínima que frena el crecimiento.
- Dilución (caldo/agar) y sistemas automatizados: determinan la CMI con métodos de dilución y lectura estandarizada; en muchos hospitales se usan sistemas automáticos, pero a menudo se complementan con técnicas como disco o gradiente cuando se necesita confirmar o ampliar información.
Los resultados se interpretan con puntos de corte clínicos y se expresan como:
- S (susceptible con pauta estándar),
- I (susceptible con mayor exposición: por ejemplo, ajustando dosis o forma de administración).
- R (resistente).
2) Pruebas rápidas de mecanismos de resistencia (minutos – <2 horas)
Buscan marcadores o actividad enzimática de resistencias relevantes (por ejemplo, β-lactamasas y carbapenemasas). Se usan cuando interesa confirmar pronto resistencias relevantes (por ejemplo, ciertas β-lactamasas/carbapenemasas) para ajustar tratamiento y medidas de control, pero no sustituyen al antibiograma completo: un resultado negativo no siempre descarta resistencia y puede requerir estudios adicionales
- Inmunocromatografía (test de “flujo lateral”): se basa en reacción antígeno-anticuerpo; es fácil de usar, no requiere equipamiento adicional y puede dar resultados en ~15 minutos. Puede detectar varios mecanismos a la vez, aunque su alcance depende de qué dianas incluya el test y de la epidemiología local.
- Pruebas colorimétricas (p. ej., Carba NP): detectan actividad enzimática (hidrólisis) mediante cambio de color; existen formatos comerciales y “caseros”, y su rendimiento puede variar según el tipo de mecanismo y la especie bacteriana.
-
3) Técnicas moleculares ygenómicas (detección de genes y caracterización avanzada)
Permiten identificar genes de resistencia más rápido que el antibiograma convencional (que requiere crecimiento bacteriano). Aportan gran valor cuando interesa confirmar pronto un mecanismo, pero no detectan todos los mecanismos y su interpretación depende del contexto clínico y del tipo de muestra.
- PCR y otros métodos moleculares (y formatos multiplex/automatizados o LAMP): permiten detectar genes de resistencia en menos tiempo que el antibiograma clásico; su utilidad depende del tipo de muestra y del panel utilizado (solo identifica lo que busca).
- Secuenciación (NGS/WGS): se emplea sobre todo para caracterizar resistencias complejas y, especialmente, para investigar brotes y cadenas de transmisión con alta precisión.
4) Espectrometría de masas (MALDI-TOF)
Su función principal es identificar la bacteria en minutos, acelerando el circuito diagnóstico. En algunos circuitos también puede ayudar a detectar de forma rápida la hidrólisis de ciertos antibióticos en ensayos específicos.
Prevención
¿Qué se puede hacer para disminuir el desarrollo de la resistencia a los antibióticos en las bacterias?
Frenar la resistencia a los antibióticos requiere un abordaje coordinado y sostenido, porque el problema se ve favorecido por varios factores: el uso inadecuado de antimicrobianos en personas y animales, la aplicación deficiente de medidas higiénicas en centros sanitarios, carencias de formación/recursos y la diseminación global de bacterias resistentes (por viajes y por la cadena alimentaria, entre otros).
Dado que la selección y propagación de resistencias es un fenómeno complejo y multifactorial, las medidas aisladas tienen menos impacto: se necesitan programas bien coordinados, con respuesta multisectorial y una perspectiva conjunta humana-veterinaria (“One Health”), en los que participen profesionales, instituciones y ciudadanía.
Prevención y control de la infección
La forma más directa de “ahorrar antibióticos” es evitar infecciones. Para ello resulta clave reforzar la higiene y el control de la infección como parte de la actividad diaria en hospitales y centros sociosanitarios, con recursos y organización adecuados.
En la comunidad, las medidas que más reducen infecciones (y por tanto tratamientos antibióticos) incluyen:
- Vacunación según recomendaciones sanitarias.
- Higiene de manos frecuente y correcta.
- Seguridad alimentaria (conservación, cocción, evitar contaminación cruzada).
- Etiqueta respiratoria (cubrir tos/estornudos, ventilación cuando proceda).
- Cuidados básicos de heridas y consulta precoz si aparecen signos de infección.
Menos infecciones implica menos tratamientos, menor presión selectiva y menor probabilidad de que aparezcan y se diseminen resistencias.
Vigilancia y sistemas de información útiles
La vigilancia permite detecta rresistencias emergentes, anticipar brotes y ajustar medidas de control. Es especialmente relevante que exista información transparente, con indicadores comunes y, cuando sea posible, en tiempo real, para conocer la situación y mejorar la respuesta.
Desde el laboratorio, la vigilancia combina:
- Seguimiento continuo de resistencias en aislamientos clínicos.
- Cultivos de vigilancia epidemiológica cuando aportan valor (por ejemplo, para investigar brotes y cortar transmisión), con utilidad demostrada en programas de control y prevención en determinados escenarios.
- Informes periódicos de sensibilidad (resúmenes locales) que orientan el tratamiento empírico y muestran tendencias de resistencia a lo largo del tiempo.
La vigilancia de las bacterias resistentes a los antibióticos existentes y emergentes es un paso importante para el desarrollo de las estrategias para luchar contra dichas bacterias. Los Centers for Disease Control and Prevention (CDC) financian diversos programas de vigilancia para monitorizar la resistencia bacteriana. Por ejemplo, el National Healthcare Safety Network (NHSN) permite a las instalaciones sanitarias comunicar las infecciones, el uso de los antibióticos y las resistencias por vía electrónica.
La Antibiotic Resistance Lab Network (ARLN) de los CDC proporciona apoyo a través de su infraestructura para la rápida detección y confirmación de las amenazas emergentes de resistencia antimicrobiana a los laboratorios de microbiología clínica de Estados Unidos, a los laboratorios comerciales y los laboratorios de salud pública del estado, ya que todos ellos están implicados en los esfuerzos de vigilancia y detección. Los CDC, la Food and Drug Administration (FDA) y el U.S. Department of Agriculture (USDA) también colaboran en el programa de monitorización de las resistencias, que a menudo se transmiten a través de la comida. En Europa, actúan el European Centre for Disease Prevention and Control (ECDC) y la Joint Action Antimicrobial Resistance and Healthcare-Associated Infections (EU-JAMRAI).
Estas redes apoyan a las instalaciones sanitarias, laboratorios, y departamentos de salud, de modo que puedan detectar los brotes de bacterias resistentes a los fármacos más rápidamente y dar una respuesta antes de que puedan extenderse ampliamente.
Optimización del uso de antibióticos
Optimizar el uso de antibióticos es una intervención esencial: no se trata de “usar menos” sin más, sino de usar mejor. En el ámbito hospitalario, estos programas se basan en un equipo multidisciplinar integrado en la institución, con objetivos claros (mejorar resultados clínicos, reducir efectos adversos, reducir resistencias y asegurar tratamientos coste-eficaces) y seguimiento mediante indicadores medibles.
En la práctica, esto se traduce en:
- Indicar antibióticos solo cuando están justificados.
- Elegir el antibiótico más adecuado (evitando espectros innecesariamente amplios).
- Ajustar dosis y duración.
- Revisar el tratamiento cuando hay resultados microbiológicos para desescalar o suspender si no procede.
Diagnóstico microbiológico precoz
Cuanto antes se identifica el agente y su sensibilidad, antes se puede evitar el antibiótico innecesario o ajustar el tratamiento. Además de los cultivos y antibiogramas, los circuitos que facilitan diagnóstico temprano y buena comunicación clínico-laboratorio reducen la duración del tratamiento empírico al mínimo imprescindible.
Innovación: nuevas tecnologías, investigación y nuevos antibióticos
Dado que la resistencia puede enlentecerse, pero no eliminarse por completo, se necesita inversión para incorporar nuevas tecnologías (prevención/control, diagnóstico precoz, administración más segura y eficaz de antimicrobianos) e impulsar la investigación y la llegada de nuevos antibióticos activos frente a bacterias resistentes.
Contribución desde la ciudadanía
La reducción de resistencias también depende de hábitos colectivos. De forma general, se recomienda:
No utilizar antibióticos para resfriados o gripe (habitualmente son infecciones víricas).
No autoprescribirse, ni compartir antibióticos, ni guardar “sobras”.
Seguir dosis y duración pautadas; no suspender el tratamiento “al encontrarse mejor” sin indicación profesional.
Mantener medidas de higiene y vacunación para reducir infecciones y contagios.
Preguntas frecuentes
¿Podría un médico recetar alguna vez un antibiótico sin hacer un cultivo o antes de tener sus resultados?
Sí. En algunas situaciones, el médico puede iniciar un tratamiento mientras el cultivo está incubándose y, en otras, puede recetar un antibiótico sin llegar a solicitar nunca un cultivo.
Aunque es imposible predecir con certeza qué bacteria está causando una infección si no se realiza un cultivo, algunos microorganismos aparecen con mucha más frecuencia que otros. Por ejemplo, la mayoría de las infecciones del tracto urinario (ITU) están causadas por la bacteria Escherichia coli. Sabiendo esto, el médico puede basarse en su experiencia para deducir qué “bicho” es el más probable y elegir un antibiótico que suele ser eficaz en la mayoría de los casos.
Además, hay infecciones potencialmente mortales que deben tratarse de inmediato, sin tiempo para esperar el resultado del cultivo. Por ejemplo, si un paciente llega con sospecha de meningitis, necesita tratamiento urgente porque se trata de una infección grave. En otras ocasiones, no se intenta el cultivo porque puede no ser posible obtener una muestra (como en la otitis media) o porque el patógeno puede ser difícil de aislar entre otros microorganismos presentes en la muestra (como en la neumonía adquirida en la comunidad). En estos casos, el médico elige un tratamiento que cubra los patógenos más frecuentes que causan esas infecciones.
¿Por qué es un gran problema la resistencia a los antibióticos?
La resistencia antimicrobiana aparece cuando las bacterias desarrollan mecanismos que hacen que los antibióticos pierdan eficacia. Esto convierte infecciones habituales en procesos más difíciles de tratar, con más complicaciones, más transmisión y peor pronóstico.
En Europa, se estima que más de 35.000 personas mueren cada año por infecciones causadas por bacterias resistentes en la UE/EEE.
En España, la SEIMC (Sociedad Española de Enfermedades Infecciosas y Microbiología Clínica) ha impulsado registros hospitalarios para estimar la carga de infecciones por bacterias multirresistentes. En el estudio SEIMC-BMR 2023, se estima que en 2023 hubo del orden de >150.000 infecciones y alrededor de 23.000 fallecimientos en los 30 días posteriores al diagnóstico (según los resultados presentados públicamente). Además, el Registro hospitalario publicado por SEIMC ya señalaba la magnitud del problema y su elevada mortalidad a 30 días.
También es un problema económico, incrementa costes directos (hospitalización, fármacos, pruebas) e indirectos (bajas laborales, pérdida de productividad). A nivel europeo, se han estimado ≈1.500 millones de euros/año en costes sanitarios y pérdidas de productividad por bacterias multirresistentes.
¿Por qué empeoran tanto estas infecciones?
Cuando un antibiótico falla, el paciente puede necesitar:
- Tratamientos alternativos (a veces menos eficaces o con más toxicidad).
- Más días de hospitalización y más riesgo de complicaciones.
- Antibióticos de “reserva”, que conviene proteger para los casos graves.
Si no podemos tratar infecciones de forma eficaz, procedimientos como cirugía mayor, quimioterapia, trasplantes o cuidados intensivos se vuelven más arriesgados, porque dependen de antibióticos que funcionen para prevenir y tratar infecciones.
¿Qué se está haciendo en España?
PRAN 2025–2027: estrategia nacional para frenar la RAM desde un enfoque integral (humana, animal y medioambiente).
Programas PROA: equipos y medidas para optimizar la prescripción y usar antibióticos cuando toca, cómo toca y el tiempo justo.
Vigilancia: redes europeas como EARS-Net y análisis integrados como JIACRA ayudan a entender tendencias de resistencias y consumo para guiar decisiones.
Mensajes para la población
- No tomes antibióticos sin receta.
- No los compartas ni guardes “por si acaso”.
- Si te los prescriben, sigue la pauta indicada.
- Prevención: higiene de manos, vacunas al día y cuidado de heridas.
Enlaces
Pruebas relacionadas:
Estados fisiológicos y enfermedades:
Noticias:
¿Usamos bien los antibióticos en España?
Resistencia cero: un 20% menos de infecciones por bacterias multirresistentes
Las “superbacterias”, creciente amenaza en Europa
En otras webs:
Ministerio de Sanidad Gobierno de España. Plan Nacional Resistencia Antibióticos
Organización Mundial de la Salud (OMS): Resistencia a los antimicrobianos
U.S. Food and Drug Administration (FDA): Antimicrobial Resistance
Antimicrobial resistance (AMR) - ECDC











